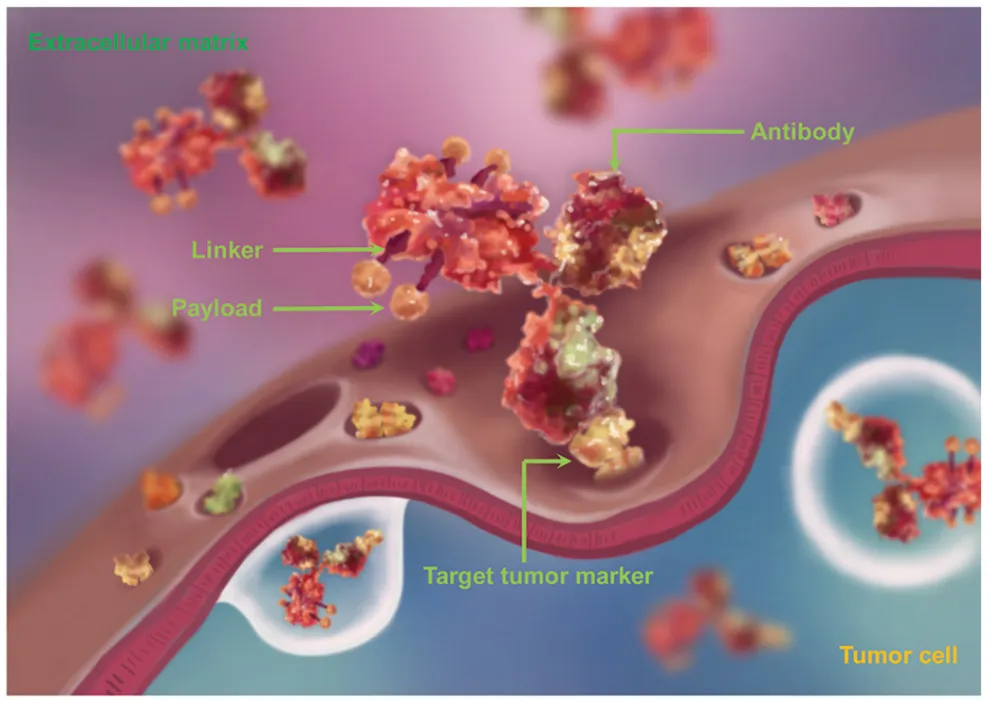
抗体偶联药物(ADC)通过“生物导弹”设计精准杀伤肿瘤细胞,其核心由靶向抗体、连接子和细胞毒性载荷三部分组成。随着技术迭代,ADC已从传统化疗升级为肿瘤靶向治疗的重要方向,并呈现多元化发展趋势。以下是主要技术路线及未来方向:
核心技术路线演进
1. 第一代ADC:探索阶段
使用鼠源抗体,易引发免疫排斥
连接子不稳定导致血液中毒素过早释放
代表药物因效力不足逐渐淘汰6
2. 第二代ADC:效能优化
抗体升级:人源化/全人源抗体降低免疫原性
毒素强化:采用微管蛋白抑制剂等高效载荷(如MMAE)
核心局限:
赖氨酸/半胱氨酸偶联导致药物抗体比(DAR)不均(通常DAR=8)
高DAR值引发血浆清除率加速和脱靶毒性46
3. 第三代ADC:精准突破
位点特异性偶联:定点修饰确保DAR均一(通常DAR=2-4)
连接子创新:可裂解连接子实现肿瘤微环境定向释放
临床成果:
截至2025年全球获批15款ADC,第三代药物占比超60%,显著提升低抗原表达实体瘤响应率。
未来发展方向
1. 载荷多元化拓展
新型毒素:开发DNA损伤剂等突破耐药机制
非毒素载荷:
AOC(抗体-寡核苷酸偶联):通过基因沉默抑制肿瘤(如siRNA递送)
ABC(抗体-聚合物偶联):增强抗体依赖性细胞毒性
2. 实体瘤治疗深化
双靶点设计克服肿瘤异质性(如HER2/HER3双抗ADC)
定点释放技术扩大“旁观者效应”,清除微转移灶
3. 技术瓶颈突破
递送系统优化:开发新型连接子降低肝毒性
冻干工艺应用:提升药物稳定性,简化冷链运输
AI驱动研发:加速生物标志物筛选与患者分层
4. 可及性提升
长效注射剂型改善治疗依从性。